CAH : Complexe argilo-humide
Chaque jardinier sait combien il est important de connaître les éléments composant les sols et la notion de CAH pour comprendre les besoins des végétaux. Les Professionnels A Domicile de la Coopérative ont décidé de voir ou revoir avec vous certaines notions élémentaires et indispensables pour vos plantes.
Composition de l’air du sol
L’air occupe tous les vides du sol, lorsque celui-ci est ressuyé. La quantité d’air contenue dans le sol dépend de sa texture, structure et de son humidité. La composition de l’air du sol est donc variable.
Comparaison de la composition de l’air atmosphérique et de l’air du sol
La respiration des racines, le métabolisme des micro-organismes aérobies et de la faune du sol consomment de l’oxygène et rejette du dioxyde de carbone.
La quantité moyenne de CO2 produite par an est de 3 à 5 g/jour/m² de sol, soit 12 à 18000kg/ha/an. Cette production varie en fonction des saisons, de la température, de l’humidité et de la nature du sol.
L’asphyxie
Les différentes formes d’asphyxie du sol
- Texture fine : Un sol fin et limoneux a tendance à se tasser sous l’effet de la pluie pour créer une croûte à la surface (battance) ce qui limite les échanges gazeux avec l’atmosphère. Le sol est donc imperméable en surface est devient asphyxiant pour les racines et les micro-organismes du sol.
- Structure compactée : Le sol est imperméable à l’eau et à l’air, il est asphyxiant pour les micro-organismes du sol et les racines. De plus le développement racinaire est difficile ainsi que le travail du sol.
- Les sols hydromorphes : Le sol est gorgé d’eau et dépourvu d’oxygène à plus ou moins long terme. Il est donc extrêmement asphyxiant pour les végétaux. Il faut procéder au préalable à des travaux d’aménagement (drainage…) pour y installer des végétaux.
Les conséquences de l’asphyxie
L’absence de microbes aérobies, qui servent d’intermédiaires entre les racines et les substances minérales et organiques, limite l’alimentation des plantes.
Les maladies fongiques (champignons) sont favorisées par l’humidité du sol et le manque d’aération.
Les propriétés chimiques des sols
Notion de chimie
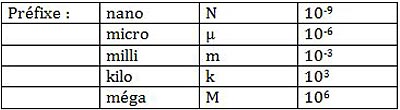
La matière est constituée d’atomes. Il existe une centaine de sortes d’atomes. Leur diamètre est d’environ 0.1 nm.
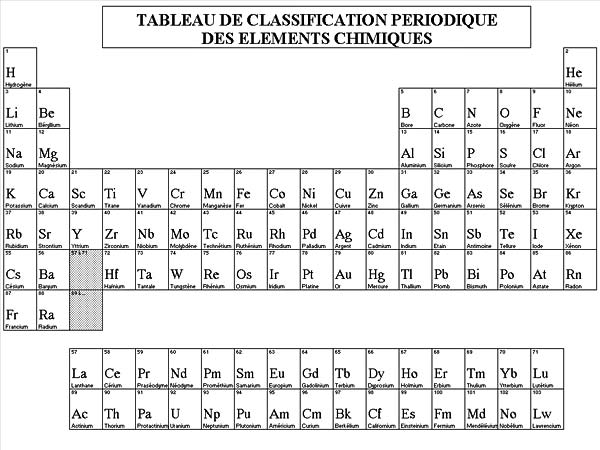
Un atome est représenté par son symbole.
Quelques symboles : H C N (azote) O Fe Cu Zn Al
La molécule
Une molécule est un assemblage fini d’atomes. Une molécule a une formule qui indique la nature et le nombre d’atomes assemblés.
Ex : Une molécule de méthane est formée de un atome de carbone et de quatre atomes d’hydrogène. (CH4)
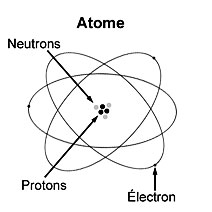
Constitution de l’atome
Un atome est formé d’un noyau positif (+), et d’électrons négatifs (-) en mouvement autour de ce noyau.
Les électrons
Ils sont tous identiques mais leur nombre varie d’un atome à un autre.
Symbole → e –
Charge → – e
Un électron porte une charge élémentaire négative.
Le noyau
Il diffère d’une sorte d’atome à une autre.
Masse de l’atome ≈ masse du noyau
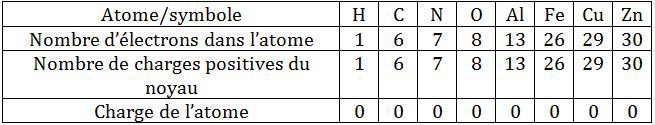
Les charges électriques dans l’atome
Dans l’atome, la charge du noyau et la charge de l’ensemble des électrons sont opposées. La charge de l’atome est toujours nulle, soit électriquement neutre.
Électriquement neutre : contient autant de charges positives que de charges négatives.
Les ions
Un ion provient d’un atome (ion monoatomique) ou d’un groupe d’atomes (ion polyatomique).
Al 3+ → l’atome d’aluminium a perdu 3 électrons
Cl – → l’atome de chlore a fixé 1 électron
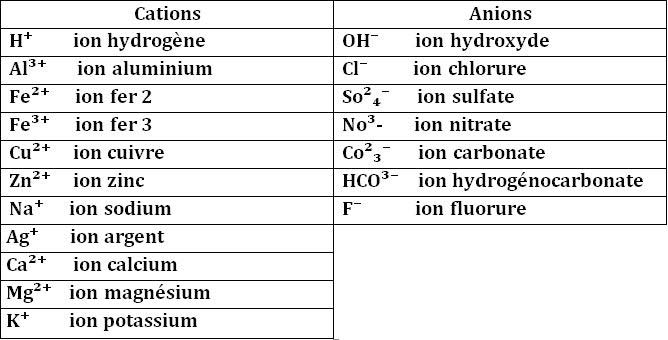
On différencie les cations (charge positive) des anions (charge négative) :
Le complexe adsorbant ou CAH
L’adsorption des cations
CAH = Complexe Argilo Humique
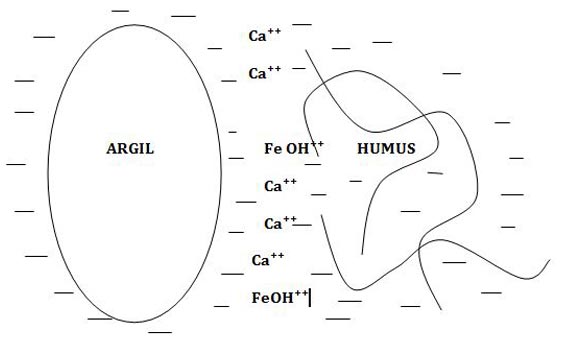
Le sol contient des colloïdes électronégatifs (l’argile et l’humus) qui retiennent à leur surface (adsorbent) des cations. Ces deux colloïdes s’assemblent malgré leurs charges identiques (puisque le – et le – se repoussent) car des cations bivalents (notamment des Ca ⁺⁺) annulent partiellement leurs charges.
Schéma du CAH
Toutes les charges négatives du CAH ne sont pas occupées par des cations bivalents (qui portent deux charges positives), certaines peuvent l’être par des cations monovalents. Tous les ions ne sont pas fixés avec la même intensité. Les ions polyvalents sont fixés plus énergiquement que les ions monovalents.
On peut donc classer ces cations selon l’intensité de leur fixation sur l’argile :
Al⁺⁺⁺, oligo-éléments dont Mn⁺⁺ Zn⁺⁺ Cu⁺⁺ > Ca⁺⁺> Mg⁺⁺> H⁺> K⁺> NH₄⁺> Na⁺
A savoir : Les oligo-éléments ne sont présents qu’en faible quantité. Al⁺⁺⁺ n’est présent que dans les sols très acides.
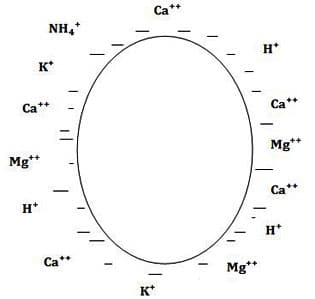
Autre représentation du CAH :
Un paramètre important du CAH des sols est le nombre de charges négatives qu’il contient. Plus ce nombre est important, plus le CAH pourra retenir des cations, ce qui est un facteur important pour la fertilité des sols. Ce nombre porte un nom, c’est la Capacité d’Echange Cationique (CEC).
Donc plus la CEC est élevée, plus le nombre de charges négatives est élevé, plus le nombre de cations est élevé.
Nb : L’unité utilisée pour la CEC est l’équivalent (eq) ou le milliéquivalent (meq).
L’adsorption des anions
La fixation des anions est un peu différente de celle des cations. En effet, les anions peuvent être fixés soit :
- Par quelques charges positives de l’argile (peu nombreuses)
- Par la présence de cations bi ou trivalents fixés sur le CAH («pont calcique»)
- Par la présence de colloïdes électropositifs comme les hydroxydes de fer et d’aluminium. Fe(OH)⁺⁺ / Fe(OH)₂⁺/ Al⁺⁺⁺.
On peut aussi classer les anions selon l’intensité de fixation :
PO₄⁻⁻, HPO₄⁻⁻ ,H₂PO₄⁻ > SO₄⁻⁻ > NO³⁻ > Cl⁻
Les ions phosphates sont aussi bien fixés que les cations, ils sont très peu mobiles dans le sol alors que les ions nitrates sont à l’inverse très mobiles : l’eau de percolation les emmène facilement. C’est le «lessivage» (d’où la pollution des nappes phréatiques en nitrates).
Echange des ions
SOLUTION DU SOL POIL ABSORBANT
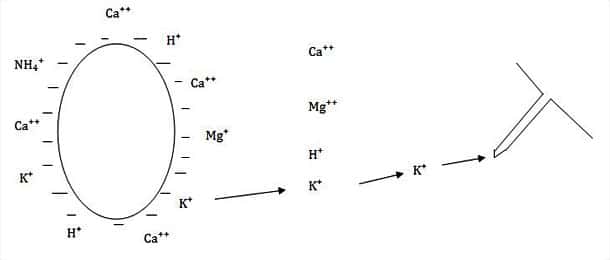
Les cations peuvent être adsorbés sur le CAH, ils peuvent aussi être libres dans la solution du sol. Ces deux milieux ne sont pas indépendants. On admet que tous les atomes sont sans cesse animés d’une frénétique agitation, c’est le mouvement brownien. Ainsi, à tous moments, des ions quittent le CAH pour aller dans la solution du sol, d’autres font l’inverse.
→ L’analogie de l’essaim d’abeilles : Au centre, la densité d’abeilles (qui marchent) est forte ; plus on s’éloigne de la périphérie, plus la densité d’abeilles (qui volent) diminue fortement ; Des abeilles volantes se posent, tandis que des abeilles posées s’envolent. En fait, les abeilles posées représentent les ions adsorbés, celles qui volent les ions libres de la solution.
L’échange des cations doit respecter : «l’équilibre des charges». Le départ du CAH d’un ion Ca⁺⁺ pourra par exemple être compensé par l’arrivée de deux ions K⁺.
Grace à ce mécanisme, les concentrations en ions de la solution du sol sont constantes, malgré d’incessants flux, puisque ses variations sont « tamponnées » par des échanges avec un stock important. Les ions sont 1000 fois plus nombreux que les ions libres dans les sols sableux et 100 000 fois plus dans les sols argileux et humifères. C’est le «pouvoir tampon» des sols.
Quand la plante puise les éléments nutritifs, la concentration de la solution du sol diminue donc le CAH libère des ions dans cette solution pour équilibrer les charges.
S’il y a un apport d’engrais alors la concentration de la solution du sol augmente donc cette solution envoie des ions au CAH afin d’équilibrer les charges.
Calcaire et calcium
Il existe d’une part le calcaire total et le calcaire actif.
- Le calcaire total représente le calcaire de «réserve» sous forme de cailloux, de graviers, de sables et le calcaire actif. Le reste du sol est constitué de matières organiques et d’argiles.
- Le calcaire actif : être actif pour le calcaire, c’est pouvoir se dissoudre rapidement dans la solution du sol, et donc apporter un fort taux d’ions calcium dans cette solution.
L’excès de calcaire actif provoque une carence induite en fer.
L’abondance de calcium (ions Ca⁺⁺) a de nombreuses conséquences sur les propriétés physiques du sol et le pH…
En climat méditerranéen, le calcium est si concentré dans la solution du sol qu’il peut se «recristalliser» pour créer une véritable barrière (de 10 cm à plusieurs mètres) à la prolifération de racines, seule une végétation xérophyte survit (thym).
On repartit les plantes en différentes catégories selon leur comportement vis-à-vis du calcium :
- Plantes calcicoles ou calciphiles ou basiphiles : elles s’accommodent de la présence de fort taux de calcium en maîtrisant l’absorption de cet ion. Elles ne sont pas exclusives au sol calcaire mais étant adaptées aux forts taux de calcium, elles deviennent plus compétitives que les autres plantes moins bien adaptées donc elles colonisent les sols calcaires majoritairement. Ex : le buis…
- Plantes calcifuges : Elles ne peuvent vivre sur les sols très calcaires, car elles ne maîtrisent pas l’absorption de l’ion calcium. En excès, il leur est toxique, et elles meurent. Ex : Châtaignier, plantes de terre de bruyère (hortensia, skimmia), sarrasin, seigle…
Les amendements
Différence entre amendement et engrais :
- Amendements : Ce sont des apports au sol en quantité importante de substances destinées à corriger des déséquilibres de structure (amélioration du CAH).
- Engrais : Ce sont des apports au sol, en quantité réduite, de substances destinées à corriger un manque d’éléments nutritifs.
Les amendements texturaux
Ce sont des amendements destinés à améliorer la texture des sols. On trouve dans cette catégorie deux composants principaux :
- Le sable, qui allège la texture des sols trop lourds (argileux).
- L’argile, qui en plus du calcium, apporte aux sols trop sableux des colloïdes afin d’améliorer la structure.
Les amendements calciques
Souvent appelés chaulage, ils permettent de corriger progressivement un sol dont le pH est acide (< à 6.5).
La quantité à apporter dépend :
- Du pH du sol
- Du pH que l’on veut obtenir
- De la nature du sol
- De l’exigence des plantes que l’on veut cultiver
On trouve le calcium sous trois formes : la chaux (CaO), le calcaire (CaCo₃) et du sulfate de calcium (CaSo₄)
En pratique, on trouve :
- Les calcaires broyés
- Les scories (produits de sidérurgie)
- Les maërls (algues broyées)
- Les sables calcaires
- La chaux vive
- La chaux éteinte
Nos pros, partout en France, se tiennent à votre disposition pour vous orienter sur la qualité de votre terrain, les espèces que vous pouvez y intégrer, contactez les !